Tenofovir
En el mundo actual, Tenofovir es un tema que ha cobrado una relevancia cada vez mayor. Ya sea por su impacto en la sociedad, su importancia en la economía o su influencia en la cultura, Tenofovir se ha convertido en un punto de atención tanto para expertos como para el público en general. Con su amplia gama de implicaciones y su capacidad de generar debate y reflexión, Tenofovir se ha establecido como un tema crucial en la agenda actual. En este artículo, exploraremos las distintas facetas de Tenofovir, analizando su origen, su evolución a lo largo del tiempo y su posible futuro. Además, examinaremos el papel que Tenofovir juega en la vida cotidiana de las personas y su relevancia en el contexto global.
| Tenofovir | ||
|---|---|---|
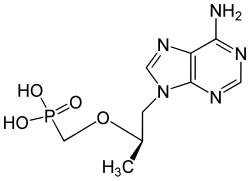 | ||
| Nombre (IUPAC) sistemático | ||
| oximetil-(propan-2-iloxicarboniloximetosi)fosforil]oximetilpropan-2-il carbonato ácido (E)-but-2-enedioico | ||
| Identificadores | ||
| Número CAS | 147127-20-6 | |
| Código ATC | J05AF07 | |
| PubChem | 464205 | |
| DrugBank | DB00300 | |
| Datos químicos | ||
| Fórmula | C9H14N5O4P | |
| Farmacocinética | ||
| Biodisponibilidad | 25% | |
| Unión proteica | < 1% | |
| Vida media | 17 horas | |
| Excreción | Renal | |
| Datos clínicos | ||
| Nombre comercial | Viread | |
| Estado legal | Necesita prescripción médica | |
| Vías de adm. | Oral | |
Tenofovir es un medicamento antiviral que se emplea para el tratamiento de la infección por el virus de la inmunodeficiencia humana (VIH), agente causante del sida, y para la infección crónica por el virus de la hepatitis B.
Historia
Fue descubierto conjuntamente por Antonín Holý del Instituto de Química Orgánica y Bioquímica de Praga, y Erik DeClercq del Instituto Rega de Investigación Médica en Bélgica. Fue aprobado por la FDA de Estados Unidos el 26 de octubre de 2001 para el tratamiento de la infección por el virus VIH y el 11 de agosto de 2008 para el tratamiento de la hepatitis B crónica.
Farmacología
Pertenece al grupo de los antirretrovirales y es un análogo de nucleótido que bloquea la acción de la transcriptasa inversa, enzima fundamental para que el virus VIH pueda replicarse.
Formas farmacéuticas
El tenofovir se administra por vía oral, se vende solo con el nombre comercial de Viread®, asociado en el mismo comprimido con emtricitabina (Truvada®), o en combinación con emtricitabina y efavirenz (Atripla®), o en combinación con bictergravir y emtricitabina (Biktarvy®).
Profilaxis pre-exposición
La asociación de tenofovir y emtricitabina (Truvada®) ha sido aprobada por la Agencia de Alimentos y Medicamentos estadounidense (FDA) para su utilización como fármaco preventivo, por ser capaz de reducir el riesgo de contraer la infección por el virus de la inmunodeficiencia humana (VIH), lo que se conoce como profilaxis pre-exposición. Su empleo está indicado en personas sanas que presenten un riesgo alto de contagiarse a través de relaciones sexuales, por ejemplo en el caso de parejas de pacientes infectados, lo que no implica que se abandonen otras medidas profilácticas, como el uso del preservativo.
Referencias
- ↑ a b c d Andrés Peralta Godoy, Ezequiel S. Vélez: Generación de recomendaciones para terapias antivirales del VIH (enlace roto disponible en Internet Archive; véase el historial, la primera versión y la última)., 4 de agosto de 2010. Consultado el 3 de julio de 2012
- ↑ a b c R. Therrien: Información sobre Tenofovir. Archivado el 4 de marzo de 2016 en Wayback Machine., 2011. Consultado el 3 de julio de 2012
- ↑ Diario El Mundo: EEUU aprueba el primer 'antisida' preventivo. Publicado el 16 de julio de 2012.